顶刊的科研天团们又双叒叕放大招啦!
抗衰老研究进入深水区:
Cell Metabolism期刊带来了NAD+研究双生花;一篇研究发现烟酸核苷堪称“NAD+充电宝”,专门给衰老过程中电量不足的细胞“续航”;另一篇则打破了“NAD不足会让肌肉变弱变老”的谣言,发现在骨骼肌中NAD+的耗竭并不会损害肌肉功能或加速衰老,颠覆以往对NAD+与肌肉衰老关系的认知。
Nature Communications论文通过单细胞代谢组学和表型分析,揭示了细胞氧化和衰老的代谢异质性;Nature Aging研究对小鼠衰老过程中脂质组景观的分析,绘制出了衰老过程中脂质代谢的动态图谱,发现糖脂代谢与肾脏炎症衰老相关。
明星分子的新作用:
Nature一文发现二甲双胍能抑制DNMT3A R882突变驱动的克隆性造血,在血液疾病防治领域取得重要进展;Redox Biology论文证实牛磺酸通过调节硫''化氢和肝细胞因子IGFBP-1改善肝损伤细胞衰老。
脂肪肝相关代谢物:
Cell Metabolism第三篇论文揭示循环甘油酸或可成为预测果糖诱导肝脂肪变性抵抗力的关键指标,这为早期识别肝病风险人群、制定个性化防治策略提供了新思路;Science研究通过大规模真菌筛查,发现肠道共生丝状真菌——嗅镰刀菌F. foetens通过次级代谢产物FF-C1通过CerS6-神经酰胺轴改善动物MASH。
导读目录
1.Cell Metabolism | 循环甘油酸可预测果糖诱导的肝脂肪变性的抵抗力
2.Cell Metabolism | 骨骼肌中NAD的耗竭不会损害肌肉功能或加速衰老
3.Nature Communications | 综合单细胞代谢组学和表型分析揭示了细胞氧化和衰老的代谢异质性
4.Cell Metabolism | 烟酸核苷维持NAD+稳态并改善与衰老相关的NAD+下降
5.Nature Aging | 小鼠衰老过程中脂质组景观分析
6.Nature | 二甲双胍抑制DNMT3A R882突变驱动的克隆性造血
7.Redox Biology | 牛磺酸通过调节硫''化氢和肝细胞因子IGFBP-1改善CCl4诱导的小鼠肝损伤中的细胞衰老
8.Science | 肠道共生丝状真菌通过次级代谢产物—CerS6—神经酰胺轴改善MASH
资源领取
本期导读文献原文,请在公众号后台回复“2025年5月绘谱导读”,即可获取资源链接。
【壹】Cell Metabolism | 循环甘油酸可预测果糖诱导的肝脂肪变性的抵抗力

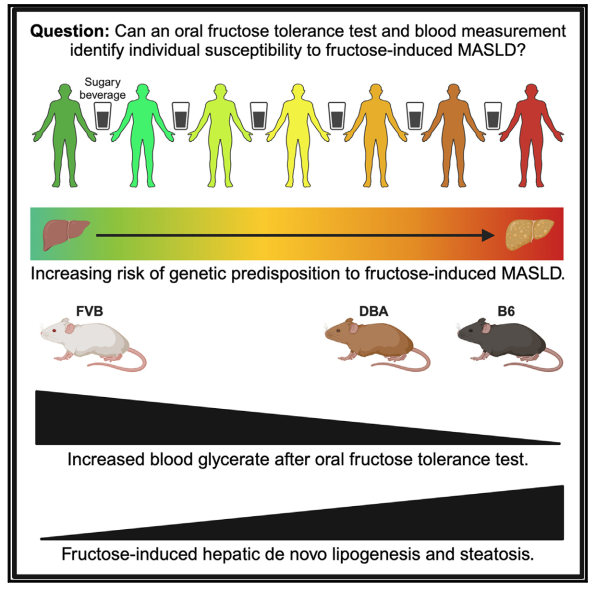
代谢功能障碍相关脂肪型肝病(MASLD)与过量果糖摄入密切相关,但其个体易感性机制尚不明确。本研究发现口服果糖耐量试验(OFTT)后循环甘油酸水平可作为预测个体对果糖诱导肝脂肪变性抵抗能力的生物标志物,揭示肠道果糖代谢能力通过抑制肝脏从头脂肪生成(DNL)介导MASLD易感性,为MASLD的个性化饮食干预提供了新方向。
①口服果糖耐量试验中甘油酸水平与肝脂肪变性的负相关性:通过对C57BL/6、DBA/2J和FVB/NJ三种品系雌雄小鼠的纵向研究,OFTT后甘油酸的AUC与12周后肝脂肪变性程度呈显著负相关,且在同品系内该相关性依然存在。¹³C果糖的同位素示踪代谢流进一步证实,抗性品系FVB小鼠肠道对果糖-甘油酸的转化效率显著高于敏感品系,其血清甘油酸水平在慢性果糖干预后较敏感品系升高6倍,且与性别无关。相比之下,果糖或葡萄糖的AUC与肝脂肪变性无显著关联,表明甘油酸是果糖代谢相关的特异性预测因子。
②甘油酸升高反映肠道果糖代谢能力增强:门静脉-体循环代谢物差异分析显示,FVB小鼠的小肠在基础状态和慢性HFCS喂养后,均表现出更强的果糖转化为甘油酸的能力。分子机制上,其十二指肠中Aldh1a1表达高、Tkfc表达低,二者比值与血清甘油酸浓度呈正相关。抗生素处理未显著影响甘油酸生成,提示宿主小肠代谢主导此通路。
③肠道果糖代谢通过抑制肝脏脂肪生成预防肝损伤:同位素示踪代谢流显示,FVB小鼠在慢性HFCS喂养后,肝脏从果糖合成脂质的能力显著降低,DNL活性及关键酶Fasn和Scd1表达未显著升高,且DNL与肝脂肪变性程度正相关。此外,FVB小鼠的空腹血糖、胰岛素及胰岛素抵抗指数(HOMA-IR)均较低,表明其代谢稳态更优。值得注意的是,FVB小鼠对高脂饮食诱导的脂肪肝仍敏感,提示果糖与脂肪的致肝损伤机制存在差异。
参考文献
Ramirez CB, Ahn IS, Rubtsova VI, et al. Circulating glycerate predicts resilience to fructose-induced hepatic steatosis. Cell Metab. 2025
【贰】Cell Metabolism | 骨骼肌中NAD的耗竭不会损害肌肉功能或加速衰老

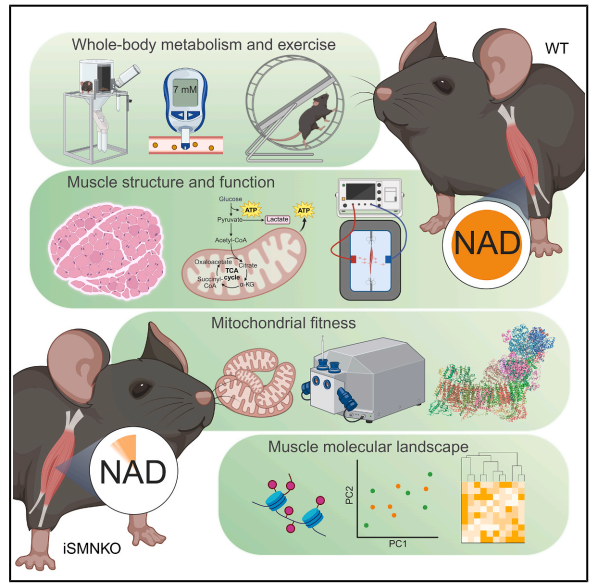
烟酰胺腺嘌呤二核苷酸(NAD+)作为能量代谢和细胞信号传导的核心分子,其耗竭常被认为与衰老及组织功能衰退相关。本研究系统探究了NAD耗竭对肌肉功能、线粒体稳态及衰老进程的影响,揭示了骨骼肌对NAD耗竭的高度耐受性,颠覆了“NAD缺失驱动肌肉衰老”的传统认知。
①骨骼肌功能对NAD耗竭的显著耐受性:通过诱导型Nampt敲除模型发现iSMNKO小鼠骨骼肌NAD+水平骤降85%,但肌纤维结构和肌力均与野生型(WT)无差异。值得注意的是,iSMNKO小鼠EDL在重复收缩中表现出更强的抗疲劳性,可能与静息状态股四头肌糖原储备增加20%及运动中糖原分解效率提升相关。运动耐力测试显示,iSMNKO小鼠运动能力未受影响,仅运动后血乳酸短暂升高,提示糖酵解代偿增强。
②线粒体功能在NAD耗竭下的稳定性机制:尽管线粒体NAD+含量降低50%,iSMNKO小鼠骨骼肌纤维的氧消耗率、内膜电位及ATP合成速率均保持正常。计算模型表明,需线粒体NAD+降至1%以下才会显著影响呼吸功能。结构上,线粒体网络形态、超复合物组成及膜脂质成分均未受影响,仅低ADP浓度下OCR轻微下降。此外,苹果酸-天冬氨酸穿梭活性维持正常,ROS生成位点转移但整体氧化应激水平未显著升高,揭示线粒体通过代谢通路重编程实现功能冗余。
③全身代谢稳态与衰老进程未受NAD长期耗竭影响:代谢评估显示,iSMNKO小鼠的体重、体成分、血糖、酮体水平及昼夜能量消耗均与WT一致,短期饮食或运动干预下代谢物调节能力未受损。老年iSMNKO小鼠肌肉NAD+水平保持稳定,未加速肌纤维萎缩或线粒体功能衰退。表观遗传时钟显示,NAD耗竭不影响生物学衰老进程。蛋白质组学分析表明,衰老相关分子变化主要由年龄驱动,而非NAD水平差异。
④代谢适应性与功能冗余的分子基础:多组学分析揭示,iSMNKO肌肉通过动态调整代谢中间产维持能量平衡,而基因表达谱和蛋白组无显著重编程。糖原代谢的优化是关键代偿策略,配合呼吸链底物灵活性和抗氧化系统微调,共同保障了功能稳定性。
参考文献
Chubanava S, Karavaeva I, Ehrlich AM, et al. NAD depletion in skeletal muscle does not compromise muscle function or accelerate aging. Cell Metab. 2025
【叁】Nature Communications | 综合单细胞代谢组学和表型分析揭示了细胞氧化和衰老的代谢异质性

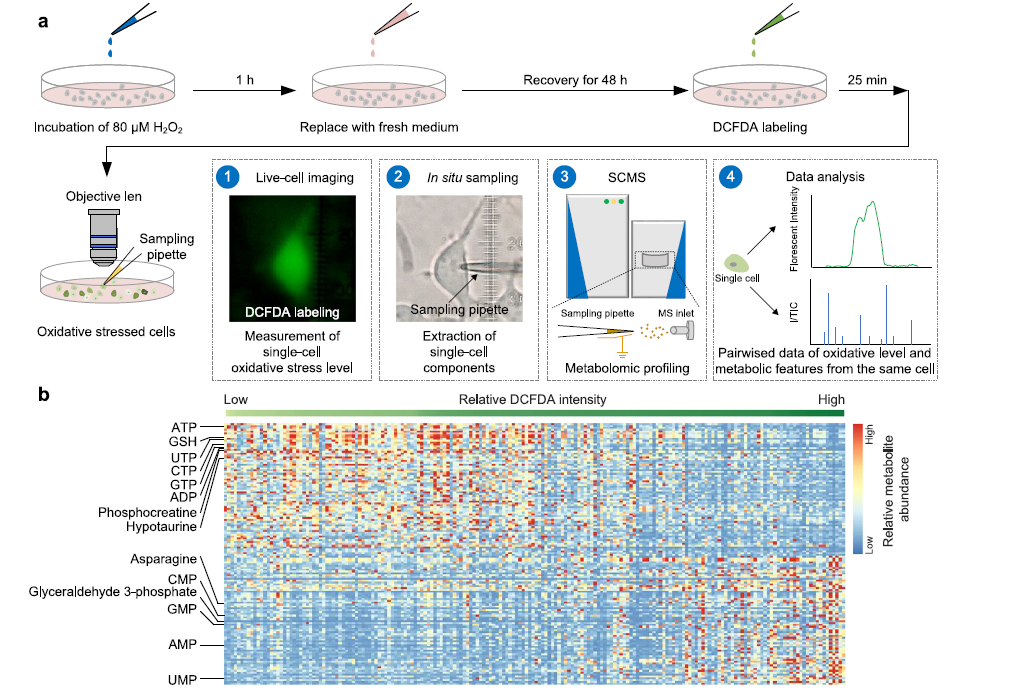
细胞衰老与氧化应激过程中存在显著的单细胞异质性,传统群体水平代谢组学难以解析其代谢异质性及与细胞表型的关联机制。本研究开发单细胞活细胞成像与质谱联用技术(SCLIMS),揭示细胞氧化应激与衰老的代谢异质性规律,发现初始代谢状态决定细胞命运,关键代谢物补充可延缓衰老进程,为相关疾病干预提供新策略。
①首先利用SCLIMS技术解析单细胞代谢组与氧化表型的跨模态关联。对HEK293T及MEFs氧化应激模型的单细胞分析显示,SCLIMS检测到>500个离子信号,确认83种代谢物。相关性分析表明,61.4%代谢物与氧化水平呈负相关,包括谷胱甘肽(GSH)、ATP、磷酸肌酸等关键代谢物。代谢通路富集显示,线粒体能量代谢、谷胱甘肽代谢及脂质代谢通路显著受氧化应激扰动。
②进一步通过k-medoids无监督聚类识别出6个代谢亚型,其氧化水平差异显著:C1亚型富含抗氧化及能量代谢物,氧化水平最低;C6亚型核苷酸代谢中间体富集,氧化水平最高。拟时序分析显示,代谢亚型从低氧化状态(C1)逐步向高氧化状态(C5/C6)分化,提示代谢引导的氧化应激动态进程。
③对初始细胞分析发现,其虽无显著氧化水平差异,但在代谢水平已存在异质性:谷胱甘肽(GSH)是区分两个细胞亚群的标志性代谢物,证实初始代谢状态决定细胞对氧化应激的响应差异。
④机器学习模型(平均AUC=0.98,r=0.88)证实单细胞代谢组可准确预测细胞氧化状态。补充SCLIMS筛选的关键代谢物(GSH、磷酸肌酸、O-磷酸乙''醇胺)可使细胞氧化水平降低67%,SA-β-Gal染色强度降低48%,线粒体膜电位恢复。
⑤最后利用秀丽隐杆线虫衰老模型进行了验证:将代谢物添加至培养基后,线虫寿命延长33%-50%,氧化损伤标志物DHE染色强度降低16%。行为学分析显示,衰老线虫的运动能能力提升,证实代谢干预对多细胞生物衰老进程的调控潜力。
参考文献
Wang Z, Ge S, Liao T, et al. Integrative single-cell metabolomics and phenotypic profiling reveals metabolic heterogeneity of cellular oxidation and senescence. Nat Commun. 2025
【肆】Cell Metabolism | 烟酸核苷维持NAD+稳态并改善与衰老相关的NAD+下降

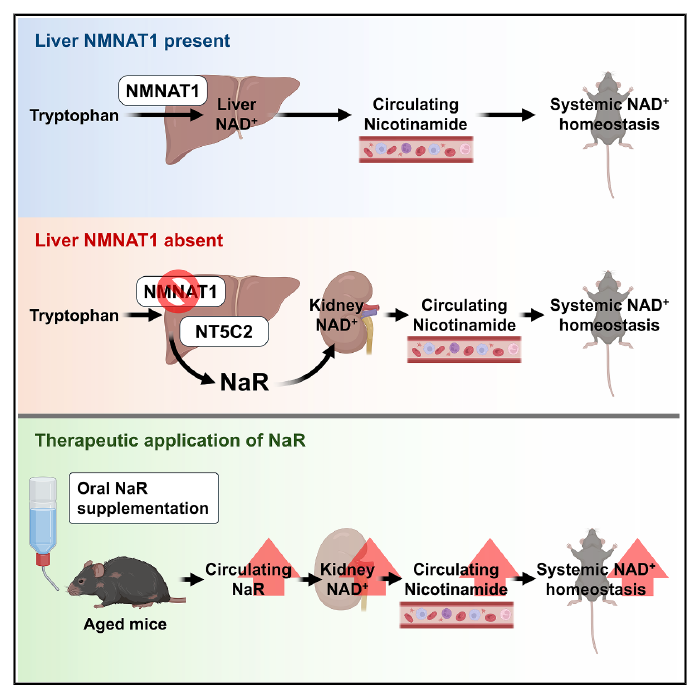
衰老相关NAD⁺稳态失衡是肾功能障碍的核心诱因,传统干预手段难以实现多器官代谢协同调控。烟酸核糖苷(NaR)通过肝-肾代谢轴维持系统性NAD⁺稳态的机制尚未明确。本研究通过多组学整合与动态同位素示踪技术,证实口服NaR可逆转衰老相关NAD⁺衰退及肾损伤,为代谢性肾病提供精准干预新策略。
①首先采用代谢组学分析发现肝特异性Nmnat1敲除小鼠(LKO)肝脏NAD⁺水平下降60%,但血清烟酰胺浓度稳定。非靶向代谢组学显示,LKO小鼠肝脏中烟酸单核苷酸(NaMN)上升30倍,并发现新型代谢物m/z 256.08(后确认为NaR),其血清浓度升高4.2倍。抗生素处理不影响NaR水平,证实其内源性合成特征。稳定同位素[U-¹³C]-色氨酸示踪显示,LKO小鼠肝脏15分钟内合成72%的M+6标记NaR,2小时后释放入血,揭示肝脏在NAD⁺合成受阻时通过NaR代偿。
②接下来通过稳定同位素示踪技术对LKO小鼠静脉注射²H₄-NaR,发现肾脏摄取NaR效率是其他器官的5.8倍,且特异性生成标记的NaAD和NAD⁺,贡献度达75%。动脉-静脉梯度分析显示,LKO小鼠肾脏净摄取NaR并释放烟酰胺。代谢通路分析证实,肾脏通过NaR→NaMN→NaAD→NAD⁺路径合成NAD⁺,其中NRK1激酶是关键酶,其敲低使NaR转化率下降91%。
③随后通过酶学干预验证了NT5C2/NRK1通路的关键作用。肝脏特异性敲低NT5C2使NaR合成减少83%,并导致肾脏NAD⁺生成下降67%。老年小鼠肝脏NaR合成能力下降54%,与色氨酸代谢关键酶QPRT表达降低2.3倍直接相关,这解释了衰老相关NAD⁺衰退的代谢根源。
④最终通过干预实验验证NaR的临床转化潜力。老年小鼠口服NaR 2周后,血清NaR水平恢复至年轻组89%,肾脏NAD+提升1.8倍,ATP含量增加62%。代谢-表型关联分析显示,肾脏NAD+水平与尿白蛋白/肌酐比呈显著负相关。组化分析证实NaR干预可降低肾脏巨噬细胞浸润,并抑制肾损伤标志物Kim1表达。
参考文献
Song WS, Shen X, Du K, et al. Nicotinic acid riboside maintains NAD+ homeostasis and ameliorates aging-associated NAD+ decline. Cell Metab. 2025
【伍】Nature Aging | 小鼠衰老过程中脂质组景观分析

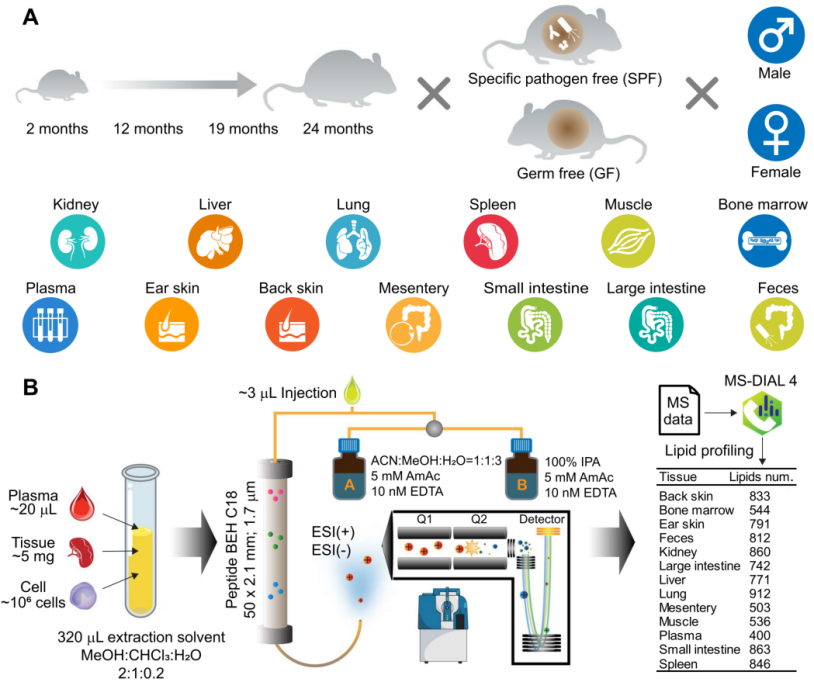
脂质在生物体中具有多样性和多功能性,可作为信号分子、能量储存分子和细胞膜成分,这些功能涉及哺乳动物细胞中的数千种脂质,脂质代谢失调与各种疾病相关,如动脉粥样硬化、癌症、非酒精性脂肪性肝炎和慢性肾脏疾病。慢性疾病的风险与衰老过程有关,了解脂质代谢的变化可能有助于阐明与衰老有关的生物机制。本研究利用脂质组学探索了小鼠衰老过程中多器官脂质的变化。
①非靶向脂质组学:分析了不同生命阶段(2、12、19和24月龄)、性别(雄/雌)及微生物状态(无特定病原体SPF或无菌GF)小鼠13种生物样本(包括肾脏、肝脏、血浆、粪便等),共鉴定出2704种脂质分子,覆盖109个脂质亚类。性别因素是造成肾脏脂质组变异的主要因素,粪便脂质组则由微生物群(SPF/GF)主导。肾脏、肺、肌肉等组织的脂质代谢与衰老高度相关。
②微生物组分析:通过16S rRNA测序分析小鼠粪便微生物组成,关联脂质组数据筛选微生物依赖性脂质。磺脂(SL)在SPF小鼠外周组织中随年龄积累,与拟杆菌门的Alistipes属丰度正相关,GF小鼠中几乎无SL;Alistipes菌属与SL(17:0;O/16:1;O)、SL(17:0;O/15:0)和SL(17:0;O/17:1;O)高度相关。肠道微生物通过调控胆汁酸(BA)去结合酶活性,影响SPF/GF小鼠的BA代谢模式(SPF小鼠以未结合BA为主,GF小鼠以结合型BA为主)。
③转录组-脂质组整合:对肾脏组织进行RNA-seq,运用加权基因共表达网络分析(WGCNA)构建基因-脂质共表达网络,并通过UGT8抑制剂(UGT8i)验证关键代谢酶的功能。抑制UGT8活性可降低雄性肾脏糖脂(GalCer、Gal2Cer)水平,减少炎症因子(Ifng、Il1b、Tnf)表达,表明糖脂代谢与肾脏炎症衰老相关。
参考文献
Tsugawa H, et al. A lipidome landscape of aging in mice. Nat Aging. 2024
【陆】Nature | 二甲双胍抑制DNMT3A R882突变驱动的克隆性造血

当造血干细胞(HSC)发生突变时,克隆性造血(CH)出现,该突变赋予了相对于野生型HSC的竞争优势,导致其克隆性扩增。具有克隆性造血的个体发生血液肿瘤和其他与年龄相关的炎性疾病的风险增加,例如,携带DNMT3A R882突变的CH患者进展为急性髓系白血病(AML)风险显著升高。本研究旨在探索抑制突变HSC竞争优势的机制,验证二甲双胍对DNMT3A R882突变驱动的CH的预防潜力。
①通过RNA-seq分析人类AML样本及小鼠模型的氧化磷酸化(OXPHOS)基因表达,利用细胞外通量分析检测线粒体呼吸功能。结果表明,DNMT3A R882突变HSPC的OXPHOS基因表达及线粒体耗氧率(OCR)显著升高,依赖线粒体呼吸获得竞争优势。敲低线粒体电子传递链亚基(Ndufv1、Cox15)可削弱突变细胞的克隆优势。
②在体外竞争实验中,二甲双胍通过抑制线粒体复合物I,降低突变HSPC的OCR和克隆形成能力。在小鼠体内,二甲双胍治疗7个月显著减少突变HSC在骨髓中的比例,抑制其长期克隆优势。
③代谢组学分析表明,二甲双胍处理增加了突变细胞中部分参与一碳代谢的代谢物水平,例如甲基化指数(SAM/SAH比值)升高。结合简化代表性亚硫酸氢盐测序(RRBS)表明,二甲双胍处理增加了突变细胞中差异低甲基化CpG位点的甲基化水平。补充外源性SAM或叶酸可模拟二甲双胍的抑制效果。
④利用Prime基因编辑技术在人类HSPC中引入DNMT3A R882突变,进行体外竞争实验。二甲双胍抑制人类突变HSPC的克隆扩增,恢复DNA甲基化和H3K27me3水平,验证其在小鼠模型中的机制同样适用于人类系统。
参考文献
Hosseini M, et al. Metformin reduces the competitive advantage of Dnmt3aR878H HSPCs. Nature. 2025
【柒】Redox Biology | 牛磺酸通过调节硫''化氢和肝细胞因子IGFBP-1改善CCl4诱导的小鼠肝损伤中的细胞衰老

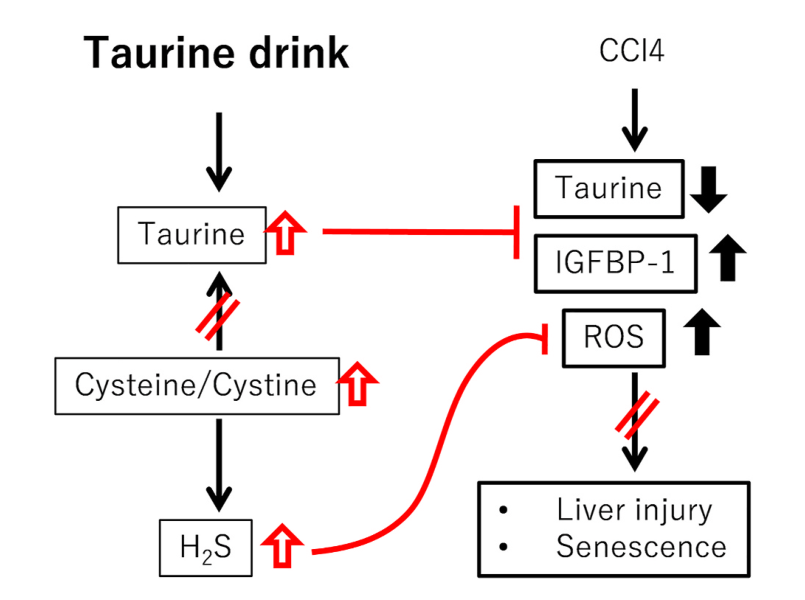
牛磺酸是一种含硫氨基酸,具有抗氧化、调节离子稳态以及大分子稳定性等功能。研究表明,牛磺酸治疗可延长小鼠的寿命和健康寿命,减轻小鼠多种组织(包括肝脏)中与年龄相关的衰老标志物的增加。因此,牛磺酸治疗可能通过减轻病理压力诱导的细胞衰老来预防疾病,但其具体机制尚未明确。该研究发现牛磺酸通过产生硫''化氢(H2S)和靶向IGFBP-1(胰岛素样生长因子结合蛋白-1)减轻慢性肝损伤的潜力。
①使用四氯''化碳(CCl4)诱导的肝损伤小鼠模型进行研究,结果发现,CCl4处理的小鼠肝脏中MDA(丙二醛)水平高于对照组,而牛磺酸处理显著降低了MDA水平。进一步检测肝功能的指标,发现牛磺酸处理显著抑制了CCl4模型中AST(天门冬氨酸氨基转移酶)和ALT(丙氨酸氨基转移酶)水平的升高。
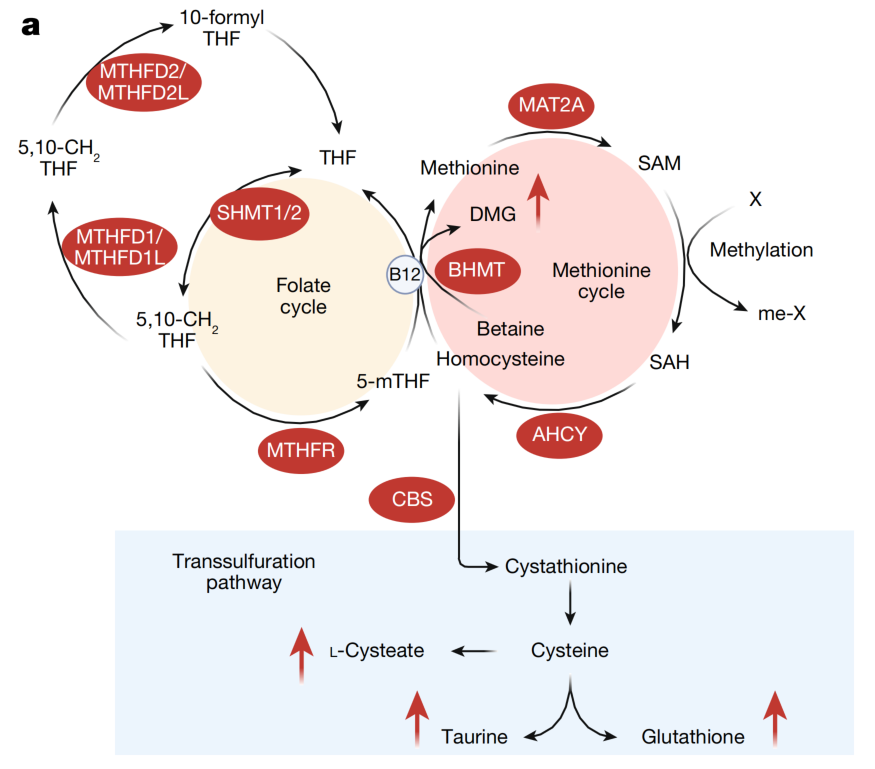
②通过研究牛磺酸处理的正常小鼠的转录组数据,发现与半胱氨酸和蛋氨酸代谢相关的基因表达变化,如半胱氨酸γ-裂解酶(Cth)、蛋氨酸腺苷基转移酶2A(Mat2a)和甜菜碱-同型半胱氨酸S-甲基转移酶(Bhmt)表达增加,而半胱氨酸亚磺酸脱羧酶(Csad)表达减少。
③通过测量小鼠肝脏中与半胱氨酸和蛋氨酸代谢相关的蛋白质和代谢物水平,结果发现在牛磺酸处理后,牛磺酸和半胱氨酸水平显著增加,且硫''化氢(H2S)水平更高。进一步研究发现,CCl4处理小鼠的胱氨酸含量降低,牛磺酸处理恢复了胱氨酸含量。
④通过研究牛磺酸处理对衰老相关分泌表型的影响,结果发现,牛磺酸处理对TGF-β1表达没有显著影响,但显著降低了IGFBP-1的表达。并且在CCl4诱导的肝脏损伤模型中,牛磺酸处理抑制了IGFBP-1 mRNA和蛋白水平的增加。
参考文献
Tsuboi A, Khanom H, Kawabata R, et al. Taurine ameliorates cellular senescence associated with an increased hydrogen sulfide and a decreased hepatokine, IGFBP-1, in CCl4-induced hepatotoxicity in mice. Redox Biology. 2025
【捌】Science | 肠道共生丝状真菌通过次级代谢产物—CerS6—神经酰胺轴改善MASH

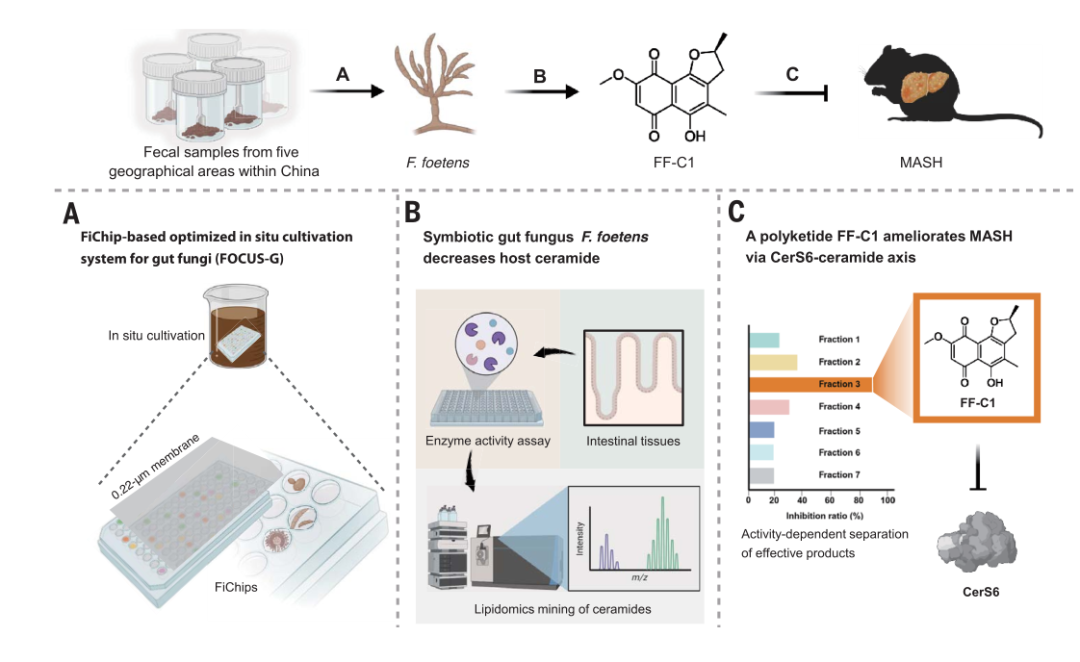
肠道微生物群与多种人类代谢疾病有关,包括代谢功能障碍相关的脂肪性肝炎(MASH)。真菌越来越被认为是这个群落的重要成员;然而,真菌共生体在代谢性疾病中的作用尚不清楚。本研究系统地分离和鉴定了肠道真菌,确定了Fusarium foetens是小鼠肠道共生丝状真菌,并且发现嗅镰刀菌F. foetens通过肠神经酰胺合成酶6 (CerS6)-神经酰胺轴逆转MASH进展,为靶向神经酰胺治疗免疫相关代谢性疾病提供新的干预策略。
①首先利用FOCUS-G(基于真菌分离芯片FiChip原位培养技术)大规模分离了来自中国5个不同地区的100份健康志愿者的粪便样本,共分离得到2137株真菌菌株。进一步测试了161个菌种的温度和氧气适应性,只有一类丝状真菌可以耐受完全厌氧的条件——镰刀菌属(Fusarium)。
②通过靶向脂质组学的分析,发现F. foetens处理显著的改变了肠道中神经酰胺框架,降低神经酰胺水平。进一步通过酶活性的检测,发现F. foetens能够降低CerS6酶活性,降低结肠中神经酰胺水平。在CDAA-HFD(胆碱缺乏氨基酸高脂饲料)诱导的SPF和GF小鼠MASH模型中, F. foetens可以显著改善肝脏脂肪变性、炎症和纤维化等MASH表型。
③通过核磁共振(NMR)和串联质谱分析技术(MS/MS)结合小鼠灌胃F. foetens后的化合物含量检测进一步鉴定,发现F. foetens产生的次级代谢物FF-C1,能够显著抑制肠道中CerS6水平以及神经酰胺的含量。
④研究团队构建了嗅镰刀菌次级代谢产物缺失的laeA基因敲除株(F. foetens-ΔlaeA)在小鼠上进行了FF-C1回补实验,证实了嗅镰刀菌确实通过FF-C1抑制肠道CerS6活性,降低神经酰胺水平,从而逆转小鼠的MASH进展。
参考文献
Zhou S, Li M, Wang P, et al. A symbiotic filamentous gut fungus ameliorates MASH via a secondary metabolite-CerS6-ceramide axis. Science. 2025
